Abbiamo parlato dell’attività fisica (leggi qui) e delle esigenze di macro e micronutrienti nel periodo gravidico (leggi qui) , oggi approfondiamo un aspetto più specifico e sicuramente meno conosciuto, il cambiamento del microbiota intestinale durante la gestazione e come influenzarlo secondo recenti ricerche.
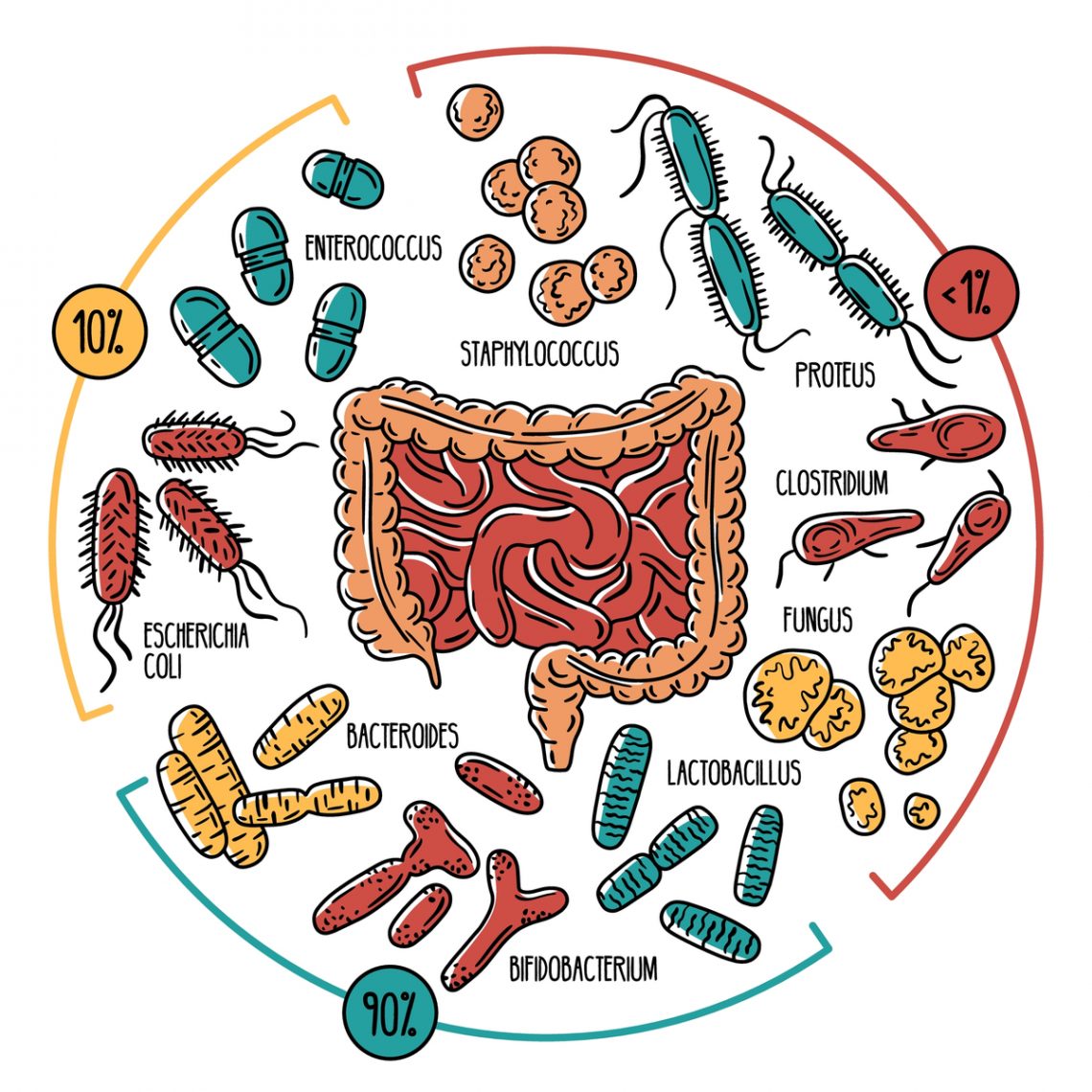
Innanzitutto è importante ricordare come i cambiamenti a cui si assiste risultano funzionali sia per la gravida sia per la trasmissione di un buon corredo microbiomiale al nascituro. Le popolazioni batteriche intestinali durante i nove mesi di gestazione si modificano portando ad un aumento dei Firmicuti, che permettono all’organismo di estrarre più efficacemente nutrienti dagli alimenti spostando la lancetta dell’organismo verso un aumento ponderale.
A livello genitale si osserva un significativo aumento di Lactobacilli. Essi saranno i primi batteri con i quali il bambino verrà in contatto in seguito a parto naturale. Questi batteri favoriscono l’immediata capacità di metabolizzare il latte materno e lo sviluppo di un sistema immunitario adeguato.
Parallelamente quando il bambino nasce attraverso parto cesareo è molto più facile che presenti immaturità nel sistema immunitario e disturbi digestivi. Tuttavia è possibile ovviare a questi problemi esponendo il neonato alla flora batterica vaginale della madre. Basta prendere una garza, impregnarla dei secreti vaginali della madre e usarla per tamponare cute, labbra, naso e orecchie del neonato appena venuto al mondo, simulandone in questo modo il passaggio attraverso le vie genitali materne (1).
Contemporaneamente i dotti galattofori delle ghiandole mammarie si arricchiscono di Bifidobacteri che nei primi 3 anni di vita costituiranno la gran parte della flora batterica che popolerà l’intestino tenue del bambino. Questo spiega l’importanza dell’allattamento al seno per lo sviluppo del microbioma del bambino. Allattamento che sempre più viene consigliato di mantenere, parallelamente all’alimentazione complementarealme, fino al 24° mese di età del bambino.
Recentemente è stato suggerito da parte dell’Organizzazione Mondiale Allergie (WAO), attraverso un documento ufficiale, l’utilizzo di probiotici durante il periodo gravidico in ottica di ridurre la probabilità di sviluppo di fenomeni allergici.
Nei bambini la prevalenza di allergie dipende nella condizione atopica dei genitori, approssimativamente risulta pari al 10% in bambini che non hanno genitori o fratelli allergici, mentre varia dal 20 al 30% in quelli con una storia atopica nel primo grado di parentela.
Le raccomandazioni della WAO sono il risultato della recente forte attenzione rivolta al microbiota intestinale, ovvero l’insieme di tutti i microrganismi presenti nel nostro intestino in un perfetto quanto delicato equilibrio. Proprio quando questo perfetto equilibrio viene perso si osservano numerose conseguenze che non si limitano all’intestino ma si ripercuotono in vari distrutti corporei. Nello specifico è stato osservato come il microbiota influenzi la sensibilizzazione o l’origine di patologie allergiche, in quanto possibile modulatore della risposta sistemica infiammatoria e immunologica.
Come è modulato il microbiota intestinale? I fattori influenti sono moltissimi, tra cui l’alimentazione, la modalità del parto, il tipo di allattamento, l’età, l’entità e il contatto con gli animali e con l’ambiente circostante, l’uso di farmaci antibiotici e il livello di attività fisica.
Vorrei soffermarmi un attimo sull’uso di antibiotici. Nel corso degli anni il loro utilizzo è aumentato a dismisura, la loro funzione è sicuramente importante in caso di infezioni batteriche, tuttavia è bene utilizzarli con oculatezza, come sempre quando si parla di farmaci. La loro azione è quasi sempre ad ampio spettro per assicurarci l’efficacia senza la necessità di analisi specifiche. Tuttavia alle volte non risolvono l’infezione proprio perché non si è individuato il ceppo batterio specifico responsabile e quindi è necessario effettuare una secondo ciclo di antibiotici e così via. Allo stesso modo capita spesso che la persona con terapia antibiotica non completi il ciclo di terapia in seguito alla scomparsa del sintomo. Questa modalità non è corretta in quanto se non si eradica completamente il batterio si ha un’alta probabilità di recidiva e soprattutto aumenta il rischio di antibiotico-resistenza, ovvero i batteri sviluppano la capacità di resistere all’antibiotico utilizzato. L’antibiotico-resistenza fa sì che la persona abbia bisogno di un antibiotico diverso o di dosi maggiori in futuro.
Tornando alla possibilità di modulare il microbiota intestinale, un’ulteriore modalità è l’utilizzo di probiotici, microorganismi viventi che quando somministrati in dosi efficaci possono conferire un beneficio salutare. Essi dono stati proposti come immuno-modulatori delle risposte allergiche interferendo con la fagocitosi e la produzione di citochine pro-infiammatorie.
Il documento presentato dalla WAO in seguito a review sistemiche di letteratura scientifica raccomanda l’utilizzo di probiotici durante la gravidanza come nel periodo dell’allattamento e la somministrazione diretta ai bambini allo scopo di ridurre il rischio di sviluppo allergico.
Gli studi hanno riportato come la somministrazione di probiotici durante la gravidanza riduca il rischio di sviluppo di allergia nei nascituri ad alto rischio. Per alto rischio si intende bambini che hanno un genitore o fratelli allergici o con una storia di rinite allergica, asma, eczema o allergie alimentare. Il beneficio netto è dovuto in primo luogo alla prevenzione di eczema, senza evidenze nette nella prevenzione di altre allergie. In questo caso i probiotici sono stati utilizzati nell’ultimo trimestre di gravidanza.
Allo stesso modo l’utilizzo di probiotici durante l’allattamento e neibambini fino ai 6 mesi di vita riduce il rischio dello sviluppo di eczema nei bambini.
Nel documento tuttavia gli stessi autori lasciano aperte alcune questioni come la possibile differenza nell’uso di probiotici naturalmente presenti nei vari alimenti o tramite l’utilizzo di integrazioni, oppure il possibile beneficio ulteriore nell’utilizzo della supplementazione probiotica quando già presenti probiotici naturali. Un’ulteriore questione aperta è la qualità dei probiotici che, come conosciamo, può modificare nettamente l’effetto finale. In questa prima revisione i ricercatori non hanno evidenziato differenze tuttavia non escludono la loro possibile presenza.
Nel 2013 alcuni psichiatri, studiando modi per migliorare la crescita cerebrale nel feto in sviluppo, hanno individuato come attraverso la somministrazione di colina si potesse prevenire lo sviluppo di alcune malattie mentali (2). La supplementazione consisteva in 3600 mg di fosfatidilcolina al mattino, una forma di colina maggiormente assorbitile a livello del flusso sanguigno, e 2700 mg alla sera. La quantità di colina somministrata era quindi di circa 900 mg, una dose doppia rispetto a quella raccomandata dalla Divisione di Salute e Medicina dell’Accademia Nazionale Americana. Dopo la nascita ai bambini sono stati somministrati 100 mg di fosfatidilcolina liquida o il placebo una volta al giorno per circa 3 mesi.
A 5 settimane dalla nascita i bambini sono stati esposti ad una serie di suoni di ticchettii in laboratorio mentre la loro attività cerebrale era monitorata attraverso elettroencefalogramma. Normalmente quando esposto a una serie di suoni in successione, il cervello dei bambini come quello degli adulti mostra una sorte di inibizione, ovvero un impulso più debole in risposta al secondo suono. Questo avviene perché realizziamo che il tono ormai familiare è insignificante.
In alcuni bambini questo non avviene, ed è stato collegato ad un aumentato rischio di problemi di attenzione, ritiro sociale e più avanti negli anni schizofrenia. Lo studio ha mostrato come il 76% dei neonati le cui madri avevano ricevuto il supplemento di colina avevano una normale inibizione allo stimolo sonoro. La percentuale scendeva al 43% in quelle che non avevano preso l’integrazione. Sembra quindi come la colina possa proteggere il cervello dei bambini dallo sviluppo di problemi mentali.
La colina è presente in numerosi alimenti. Le uova, il pesce e il fegato ne sono particolarmente ricchi.
La presenza di pochi studi a riguardo non permettono ancora di avere delle raccomandazioni precise riguardo alla supplementazione di colina. Alcuni studi condotti dalla Dott.ssa Monk della Columbia University mostrano come un’alimentazione ottimale, comprendente colina e un’adeguato ammontare di zinco e acidi grassi della serie omega-3 possano avere benefici nella salute e sviluppo cerebrale.
L’importanza di un perfetto equilibrio del microbiota è messo in evidenza anche da studi che riportano un’associazione tra alcuni disturbi mentali come autismo e schizofrenia e infezioni di patogeni microbici durante il periodo perinatale (3) (4).
Bibliografia:
- Dominguez-Bello M. G., et al, Delivery mode shapes the acquisition and structure of the initial microbiota across multiple body habitats in newborns, 2010, PNAS.
- Freedman R. et al, Perinatal Choline Effects on Neonatal Pathophysiology Related to Later Schizophrenia Risk, 2013, The American Journal of Psychiatry.
- Finegold SM, et al., Gastrointestinal microflora studies in late-onset autism, 2002, Clin Infect Dis 35 (Suppl 1):S6–S16.
- Mittal VA, Ellman LM, Cannon TD Gene-environment interaction and covariation in schizophrenia: The role of obstetric complications, 2008, Schizophr Bull 34:1083–1094.


